NHẬP KHẨU VÀ XUẤT KHẨU GĂNG TAY Y TẾ, GĂNG TAY CAO SU THEO QUY ĐỊNH MỚI NHẤT 2021
[Luật Đông Á] Ngày 7/12/2020, Bộ công thương ban hàng Thông tư 44/2020/TT-BCT về việc cấm tạm nhập, tái xuất 3 mặt hàng: Găng tay y tế, Khẩu trang y tế, Bộ trang phục phòng chống dịch- Thuộc nhóm trang thiết bị y tế loại A. Theo đó, Luật Đông Á xin cập nhật đầy đủ các quy định để doanh nghiệp, tổ chức kinh doanh và hoạt động trong lĩnh vực này hiểu rõ, hiểu đúng và thực hiện đúng các quy định của pháp luật hiện hành.Căn cứ theo nội dung của Thông tư 44/2020/TT-BCT kể từ ngày 22/01/2021 đến hết ngày 31/12/2021 doanh nghiệp kinh doanh trong lĩnh vực tạm nhập, tái xuất các sản phẩm găng tay y tế, Khẩu trang y tế, Bộ trang phục phòng, chống dịch (gồm quần áo, kính, khẩu trang y tế, mũ bảo hộ, găng tay, giày) sẽ KHÔNG được tạm nhập tái xuất tự do như trước đây nữa. Vậy để hiểu rõ chúng ta cần làm rõ các khai niệm và các nội dung cụ thể như sau:
Tạm nhập, tái xuất là gì:
+Tạm nhập: Là việc Thương nhân Việt Nam đứng ra nhập khẩu hàng hóa trong một thời gian ngắn hạn (“tạm”) vào lãnh thổ Viêt Nam. Thông thường, hàng hóa sau khi được nhập khẩu vào một quốc gia thì sẽ được lưu lại tại quốc gia đó để phân phối ra thị trường hoặc phục vụ cho một mục đích nhất định của doanh nghiệp nhập khẩu trong sản xuất kinh doanh và có lưu thông trên thị trường Việt Nam. Tuy nhiên, với trường hợp tạm nhập thì hàng hóa nhập khẩu không nhằm mục đích cho lưu thông tại thị trường Việt Nam mà sau một thời gian ngắn được xuất khẩu sang nước thứ ba.
+Tái xuất: Là quá trình tiếp sau của tạm nhập. Sau khi hàng hóa được làm thủ tục thông quan, nhập khẩu vào lãnh thổ Việt Nam thì thương nhân thực hiện việc tạm nhập sẽ xuất khẩu hàng hóa đó lại tới một quốc gia khác. Bản chất, hàng hóa này được xuất khẩu hai lần, xuất khẩu đi từ nước đầu tiên sau đó tạm nhập khẩu vào Việt Nam và lại xuất khẩu sang một nước khác nên gọi là tái xuất.
Căn cứ vào Thông tư 44/2020/TT-BCT ban hành ngày 07/12/2020 và có hiệu lực từ ngày 22/01/2021 và hết hiệu lực vào ngày 31/12/202;

Tạm ngừng kinh doanh Tạm Nhập, Tái Xuất mặt hàng Găng Tay Y Tế
Doanh nghiệp sẽ KHÔNG được nhập khẩu găng tay y tế với mã HS là: 3926.20.90; 4015.11.00; 4015.19.00;
Theo đó, doanh nghiệp sẽ hoàn thiện hồ sơ và nhập khẩu về dưới dạng là:
Phương tiện bảo vệ tay (Găng tay bảo hộ lao động chống đâm thủng, cứa rách, chống cháy, cách điện, chống hóa chất) có mã HS code:
3926.20.60
3926.90.39
4203.29.10
6116.10.90
6116.99.00
6216.00.10
6216.00.99
Căn cứ theo quy định của Thông tư 22/2018/TT-BLDTBXH.
Lưu ý: Cho tới thời điểm hiện tại, các quy định pháp luật hiện hành chưa có văn bản quy định rõ ràng về khái niệm găng tay y tế mà chỉ được phân biệt ra làm 2 loại: Găng khám bệnh sử dụng 1 lần được xếp vào nhóm trang thiết bị y tế loại A (Theo quy định tại TCVN 64343-1 và 6343-2)- Nhóm mà tất cả các doanh nghiệp Việt Nam đang xin giấy phép để lưu hành trong nước và xuất khẩu; Găng phẫu thuật sử dụng 1 lần được xếp vào nhóm trang thiết bị y tế loại B (TCVN 6344:2007).
Như vậy, căn cứ theo quy định của pháp luật hiện hành, doanh nghiệp cần làm các hồ sơ sau:
Thứ nhất: Doanh nghiệp tiến hành nhập khẩu găng tay cao su đến trước ngày 22/01/2021. Từ 22/01/2021, Doanh nghiệp sẽ cần phải đảm bảo báo cho các nhà sản xuất làm hồ sơ tên sản phẩm nên chỉ để là: Găng tay hoặc găng tay Nitrile không bột….đưa sản phẩm về mã HS theo quy định Thông tư 22/2018/TT-BLDTBXH mà chúng tôi đề xuất ở trên.
Thứ hai: Trường hợp doanh nghiệp bán trong nước cho các doanh nghiệp/ tổ chức khác để là găng tay khám bệnh thì doanh nghiệp cần tiến hành làm các thủ tục bên Sở Y tế.
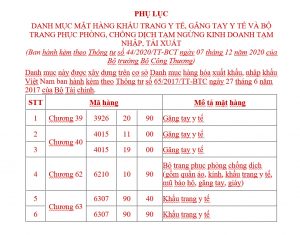
Danh mục mặt hàng Khẩu Trang Y Tế, Găng Tay Y Tế, Bộ Trang Phục Phòng Chống Dịch tạm ngừng kinh doanh, tạm nhập tái xuất
Thủ tục trong nước sẽ xảy ra 2 trường hợp:
TRƯỜNG HỢP 1:
Làm theo quy định Thông tư 22/2018/TT-BLDTBXH
Bước 1: Chú ý việc đặt tên sản phẩm là: Găng tay hoặc găng tay Nitrile không bột,… xin cấp chứng nhận Hợp chuẩn theo TCVN 8838- 1, 2, 3:2011 và QCVN 24: 2014/BLĐTBXH;
Bước 2: Nộp hồ sơ công bố hợp chuẩn và xin cấp Giấy chứng nhận lưu hành tự do cho sản phẩm do Bộ Lao động Thương Binh và xã Hội cấp phép;
TRƯỜNG HỢP 2:
Quý khách muốn để tên sản phẩm là Găng tay khám bệnh Nitrile không bột dùng 1 lần thuộc nhóm Trang thiết bị y tế loại A:
Bước 1: Xin cấp chứng nhận ISO 13485 (trong trường hợp: Doanh nghiệp/ tổ chức đã có mã ngành nghề, ĐKKD của nhà xưởng): Nhà xưởng được xây dựng theo tiêu chuẩn đạt chuẩn về sản xuất trang thiết bị y tế loại A, Hợp đồng mua bán nguyên liệu, hệ thống máy móc, Nhân sự (bằng dược, trung cấp các ngành y, dược, trang thiết bị y tế);
Bước 2: Công bố đủ điều kiện sản xuất trang thiết bị y tế loại A tại Sở Y tế nơi doanh nghiệp/ tổ chức xây dựng nhà xưởng;
Bước 3: Kiểm nghiệm và phân loại sản phẩm trang thiết bị y tế loại A. Việc thử nghiệm sản phẩm doanh nghiệp/ tổ chức có thể liên hệ và tiến hành làm ở nhiều đơn vị trong nước (lưu ý: Đây là hồ sơ trong nước nên tất cả các bản báo cáo test ở nước ngoài đều không có hiệu lực tại Việt Nam) có đủ chức năng và thẩm quyền tiến hành công việc này nên doanh nghiệp có nhiều sự lựa chọn tối ưu về chi phí và thời gian cũng như việc đi lại được thuận tiện hơn;
Bước 4: Công bố áp dụng sản phẩm trang thiết bị y tế loại A tại Sở Y tế nơi trụ sở chính của DN;
Bước 5: Xin cấp chứng nhận lưu hành tự do (Certificate Of Free Sale- CFS) tại Bộ Y tế. Doanh nghiệp cần đảm bảo rằng phải có nhà máy, hệ thống máy móc trang thiết bị đạt chuẩn, nhân sự và máy móc tiệt trùng cho sản phẩm;
Lưu ý: Giấy chứng nhận lưu hành tự do này chỉ dùng cho mục đích xuất khẩu
